Restriktivní kardiomyopatie
Definice
Restriktivní kardiomyopatie (RKMP) je charakterizována abnormální diastolickou funkcí se ztluštělými nebo rigidními stěnami komor, což vede ke zvýšení plnicích tlaků levostranných nebo pravostranných srdečních oddílů.
Etiologie
Existuje celá řada onemocnění, která mohou způsobit restriktivní kardiomyopatii, včetně infiltrativních onemocnění, střádavých onemocnění a různých systémových onemocnění.
Mezi tři hlavní příčiny RKMP patří srdeční amyloidóza, srdeční sarkoidóza a srdeční hemochromatóza.
Obrázek 1 Příčiny restriktivní kardiomyopatie
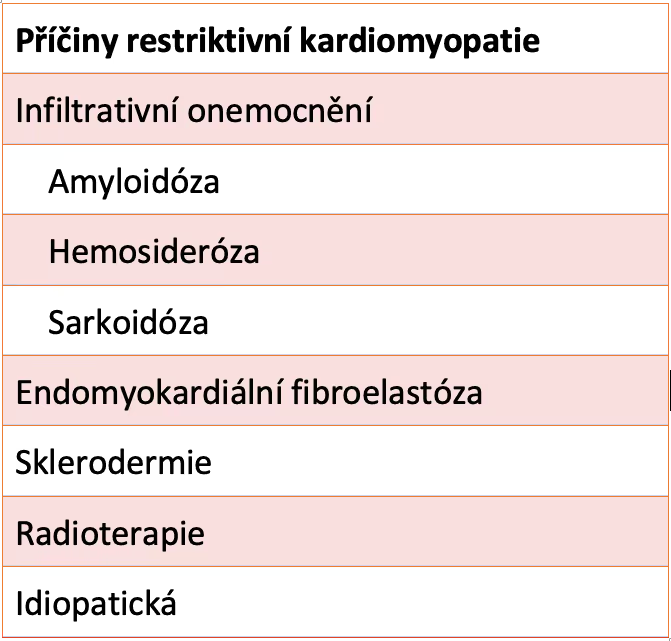
Patofyziologie
Většina restriktivních kardiomyopatií je způsobena infiltrací abnormální tkání mezi myocyty, ukládáním abnormálních metabolických produktů uvnitř myocytů nebo fibrotickým poškozením.
Je charakterizována zvýšenou tuhostí myokardu, která způsobuje náhlé zvýšení tlaku v komoře při jen malém zvětšení objemu.
Klinické projevy
Při postižení jedné nebo obou komor může RKMP způsobit příznaky nebo symptomy selhání levé a/nebo pravé komory srdeční. Jedná se o zvýšenou náplň krčních žil, ascites, otoky dolních končetin a méně často plicní edém.
Někdy se vyskytuje synkopa, často námahová, která odráží omezenou schopnost srdce zvýšit diastolickou náplň.
Někteří pacienti si stěžují na horší toleranci námahy nebo je u nich nově diagnostikována arytmie, nejčastěji fibrilace síní. V méně šťastných případech se u některých projeví náhlou srdeční smrtí (SCD).
Když vyšetřujeme pacienta s podezřením na RCM, je důležité pátrat po extrakardiálních projevech, jako jsou karpální tunel, který může být přítomen u amyloidózy, nebo oboustranné infiltráty v oblasti plicních hilů, které se vyskytují u sarkoidózy. Hemochromatóza se typicky projevuje klasickou bronzovou kůží, cirhózou, artralgiemi a někdy endokrinopatiemi jako diabetes mellitus z depozit ve slinivce břišní.
Echokardiografické nálezy restriktivní kardiomyopatie
Kompletní posouzení srdeční amyloidózy je popsáno v kapitole nazvané Amyloidóza.
1. Hodnocení tloušťky levé a pravé komory
Levá i pravá komora jsou často zesílené, ale není to podmínkou.
Obvyklým nálezem je malá levá komora (není dilatovaná) s výraznou dilatací síní a normální systolickou funkcí.
Průměr stěny LK lze měřit ze projekcí PLAX nebo PSAX.
Relativní tloušťka stěny LK - (IVS+PWT)/LVEDD = >0,6 (IVS = interventrikulární septum, PWT = tloušťka zadní stěny).
Video 1 Restriktivní KMP, projekce A3C - malá LK s koncentrickou hypertrofií, jiskřivý/zrnitý myokard LK a masivně dilatovaná LS.

Obrázek 2 Hypertrofie stěny LK při RKMP, projekce A3C - koncentrická hypertrofie zejména zadní stěny LK - 19 mm.

Obrázek 3 Hodnocení globálního longitudálního strainu u RKMP - výrazně snížený GLS -11,7 %, hypokineza přední stěny a snížená podélná kontraktilita zejména v bazálních segmentech - typicky bez postižení apikálních segmentů (tzv. apical sparing).

Obr. 4 Měření amplitudy systolické exkurze roviny mitrálního anulu (MAPSE) u RKMP, septální (vlevo) a laterální (vpravo) - MAPSE odráží globální longitudinální funkci LK, MAPSE ≥ 10 mm znamená zachovalou ejekční frakci, < 8 mm znamená zhoršenou a < 7 mm těžce zhoršenou funkci levé komory. Tento pacient má septální MAPSE 6 mm a laterální 7 mm.

Video 2 3D hodnocení ejekční frakce u RCM s difuzní hypokinezí LK - mírně snížená EF (41 %), ale významná systolická dysfunkce se srdečním indexem (CI) = 1,3 l/min/m2.

2. Hodnocení vzhledu myokardu
Myokard se jeví jako "zrnitý" nebo "jiskřivý" (jako broušené sklo) kvůli hyperechogenitě myokardiálního infiltrátu.
Video 3 Amyloidóza srdce, projekce PLAX - pacient s potvrzenou AL amyloidózou s typickými echokardiografickými známkami amyloidové infiltrace myokardu. Na videu níže je vidět hypertrofická boční stěna a interventrikulární septum s charakteristickým zrnitým nebo skvrnitým vzhledem myokardu a poruchou pohybu bazálních segmentů LK.

Video 4 RKMP, projekce A3C - denzní spontánní echokontrast LK, silně kalcifikované části LK vytvářejí jiskřivý vzhled myokardu.

3. Hodnocení objemu levé a pravé síně
Při RCM se levá síň často zvětšuje.
Obrázek 5 Extrémně dilatovaná LK při RKMP, Simpsonova biplanární metoda v projekcích A4C a A2C - plocha A4C - 51,0 cm2, A2C - délka 99 mm, plocha A2C - 52,0 cm2, LAVi 160,5 cm3

Video 5 RKMP, dilatovaná LS a PS - LS výrazně dilatovaná (LAVi 71,8 cm3/m2) a pravá síň (plocha 33 cm2).

4. Dopplerovské hodnocení rychlostí v oblasti mitrálního anulu
Rychlost v oblasti mitrálního anulu měřená dopplerovskou echokardiografií se používá k hodnocení diastolické funkce levé komory.
U RKMP ukazuje PW-Doppler z mitrální chlopně "restriktivní tvar" s velmi vysokou časnou diastolickou rychlostí (vlna E), krátkým časem zpomalení (<160 ms), nízkým pozdním diastolickým plněním (vlna A) transmitrální rychlosti, což svědčí o zhoršené diastolické funkci levé komory se zvýšenými plnicími tlaky.
Obrázek 6 Dopplerovské nálezy u RKMP

Obrázek 7 Restriktivní kardiomyopatie vs. konstriktivní perikarditida: stručný přehled
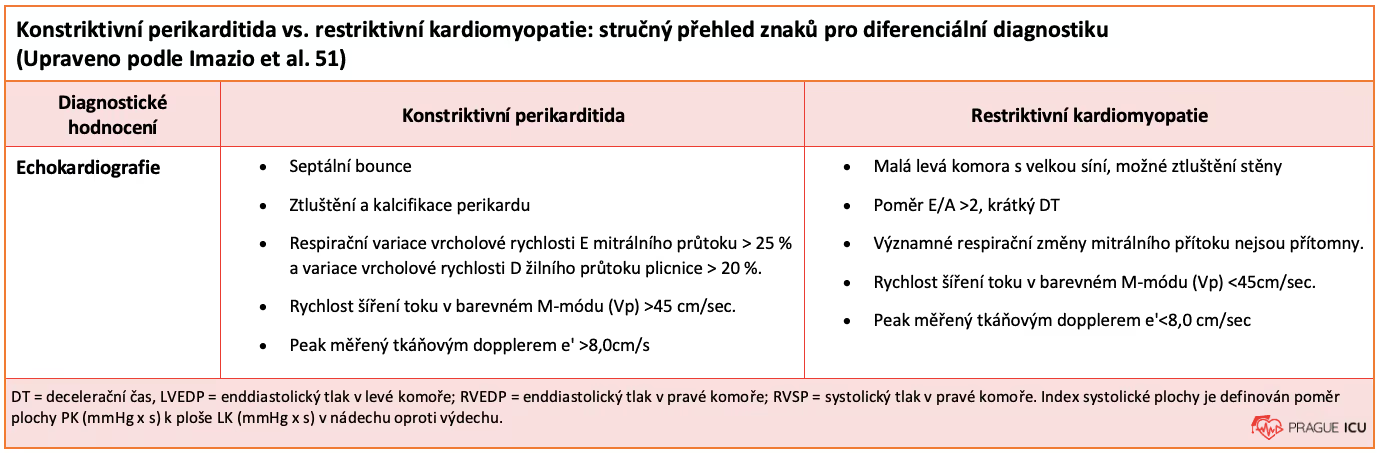

Obrázek 9 PW dopplerovské měření mitrálního průtoku v RKMP, restriktivní tvar plnění - poměr E/A 4,00, E/e' je 19,5, zkrácená decelerační doba (85 ms).

Obrázek 10 Tkáňový doppler septální (vlevo) a laterální (vpravo) u RKMP, diastolická dysfunkce IV. stupně - snížené e' septální - 3 cm/s, e' laterální - 8 cm/s. E/e' = 19,5

Amyloidóza
Je onemocnění charakterizované extracelulárním ukládáním amyloidu, který je tvořen chybně složenými produkty z proteinových prekurzorů.
V závislosti na typu amyloidózy (to znamená, jaký typ amyloidu se ukládá) může postihovat různé orgány a může se týkat i srdce.
Postižení srdce se nejčastěji vyskytuje u následujících pěti typů amyloidózy: amyloid s lehkým řetězcem (AL), amyloid odvozený od wild-type transthyretinu (TTRwt), mutantní TTR (ATTRm neboli familiární amyloidóza), lokalizovaná ložiska amyloidu v síních odvozená od síňového natriuretického peptidu a vzácně sekundární (AA) amyloidóza (odvozená od zánětlivého proteinu sérového amyloidu A).
Téměř všechny případy klinické srdeční amyloidózy (> 95 %) jsou způsobeny amyloidózou lehkých řetězců (AL) a transthyretinovou amyloidózou (ATTR), protože lokalizovaná depozita síňového amyloidu odvozená od síňového natriuretického peptidu nemají žádný vliv na přežití a není nutná žádná léčba.
Nejčastějším projevem srdeční amyloidózy je srdeční selhání v důsledku restriktivní kardiomyopatie.
Obrázek 11 Typy amyloidózy, které postihují srdce
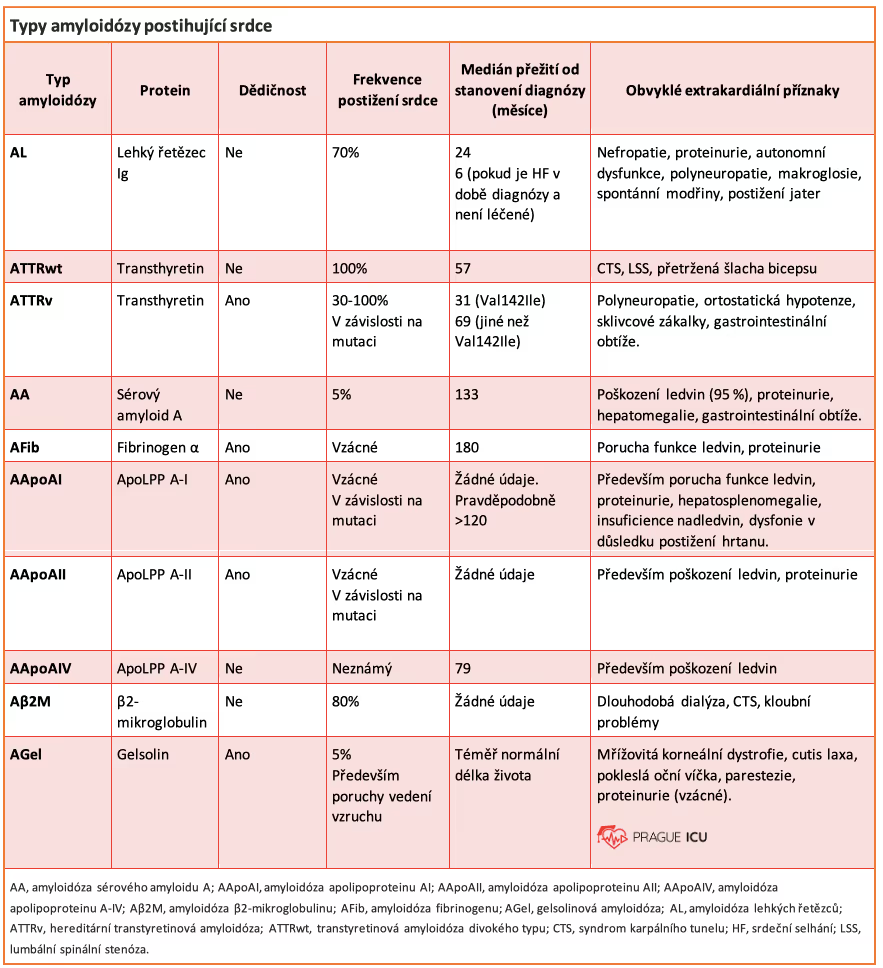
Převzato z: Garcia-Pavia P, Rapezzi C, Adler Y, et al. Diagnosis and treatment of cardiac amyloidosis: a position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2021 Apr 21;42(16):1554-1568. doi: 10.1093/eurheartj/ehab072.
AL amyloidóza
Prekurzorovým proteinem AL amyloidózy je abnormální lehký řetězec produkovaný dysfunkčními plazmatickými buňkami.
AL amyloidóza je spojena s mnohočetným myelomem a její diagnostika a léčba vyžaduje multidisciplinární přístup.
AL amyloidóza může postihnout téměř všechny orgány s výjimkou centrálního nervového systému.
Obvyklý věk při nástupu onemocnění je > 50 let a jedná se o vzácné onemocnění s výskytem přibližně 2 500 až 5 000 nových případů v USA ročně.
Amyloidóza ATTR
ATTR amyloidóza může být dědičné nebo získané onemocnění.
Dědičná ATTR amyloidóza je způsobena genetickou mutací v genu kódujícím transthyretin.
Hlavní fyziologickou funkcí transthyretinu je transport hormonu štítné žlázy a také vitaminu A (retinolu). Nebylo však prokázáno, že by amyloidóza ATTR byla spojena s patologií štítné žlázy nebo vitaminu A.
Wild-type (nedědičná) ATTR amyloidóza obvykle postihuje starší muže a projevuje se srdečními příznaky.
Jedná se o nejčastější srdeční amyloidózu.
Prevalence wild-type ATTR amyloidózy se zvyšuje s věkem, přičemž téměř všichni pacienti jsou starší 60 let.
Klinický obraz a diagnostika
Srdeční amyloidóza se typicky projevuje příznaky a projevy srdečního selhání s výraznými rysy selhání pravé komory včetně:
- otoků dolních končetin
- zvýšenou náplní krčních žil
- jaterním městnáním a ascitem
- dušností
Pokud je navíc postižen převodní systém, mohou pacienti udávat synkopu nebo presynkopu. U různých typů amyloidózy mohou být přítomny odlišné extrakardiální příznaky. Extrakardiální příznaky jsou shrnuty v následující tabulce.
Obrázek 12 Klinické projevy AL a ATTR amyloidózy
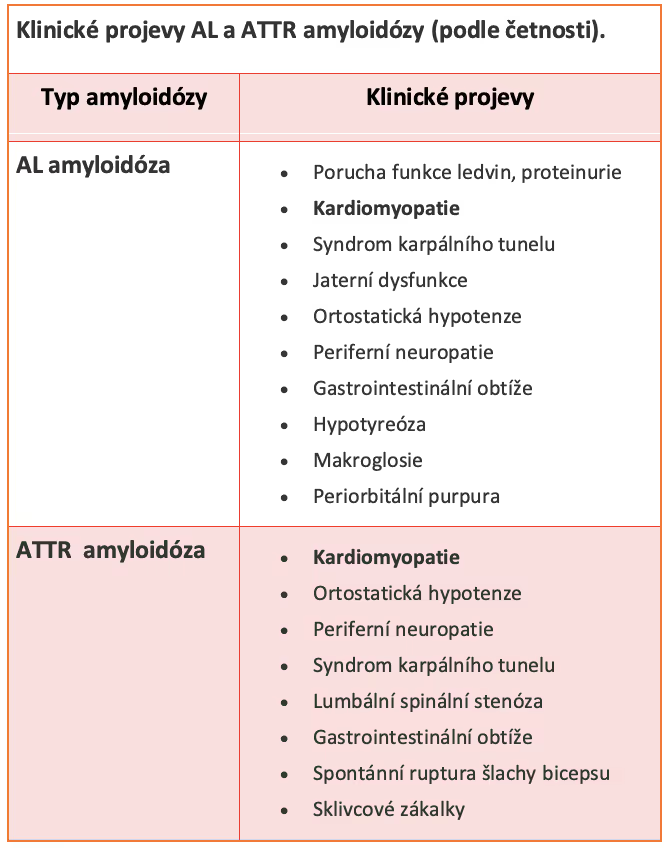
Převzato z: Georgios Papingiotis; Lamprini Basmpana, Dimitrios Farmakis, Cardiac amyloidosis: epidemiology, diagnosis and therapy, e-Journal of Cardiology Practice, Vol. 19, N° 19 - 21 Apr 2021, available from: https://www.escardio.org/Journals/E-Journal-of-Cardiology-Practice/Volume-19/cardiac-amyloidosis-epidemiology-diagnosis-and-therapy
EKG
EKG znaky AL amyloidózy zahrnují:
- Nízká voltáž v končetinových svodech
- Osa doprava
- AV blokáda 1. stupně
- Q vlny ve svodech V1 až V3
- Blokáda levého raménka je u AL amyloidózy vzácná
U ATTR amyloidózy:
- Normální voltáž
- Nespecifická porucha vedení
- Změny vlny ST-T
- Blokáda levého raménka je častější
- Zejména u ATTRwt se s postupujícím onemocněním může objevit AV blok vyššího stupně
Echokardiografie
Seznam možných nálezů při transtorakální echokardiografii amyloidózy zahrnuje:
- Ztluštění levé komory
- Zrnitý nebo jiskřivý vzhled myokardu sekundárně způsobený ukládáním amyloidu v myokardu
- Ztluštění interventrikulárního septa
- Diastolická dysfunkce
- Normální nebo zmenšená dutina LK
- Perikardiální výpotek (obvykle malý)
- Hypertrofie pravé komory
- Zvětšení levé síně
- Ztluštělé atrio-ventrikulární chlopně
- Dilatace pravé komory (ukazuje na špatnou prognózu)
- Dynamická obstrukce výtokového traktu levé komory
- Disociace mezi krátkou a dlouhou osou systolické funkce.
- Intrakardiální trombus jako důsledek špatné funkce LK a zejména je-li přítomna fibrilace síní
Echokardiografická diagnostická kritéria navržená ESC z (obrázek 13):

Převzato z: Garcia-Pavia P, Rapezzi C, Adler Y, et al. Diagnosis and treatment of cardiac amyloidosis: a position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2021 Apr 21;42(16):1554-1568. doi: 10.1093/eurheartj/ehab072. PMID: 33825853; PMCID: PMC8060056.
Typickým echokardiografickým nálezem pro srdeční amyloidózu je ztluštělá stěna levé komory (> 12 mm).
Často lze pozorovat i další nálezy, jako je zvětšení levé síně, které však stejně jako ztluštění stěny nejsou pro srdeční amyloidózu specifické. Diferenciální diagnóza zahrnuje hypertenzi, obstrukci průtoku při aortální stenóze nebo hypertrofickou kardiomyopatii a další.
Z hlediska funkce komor se obvykle zjišťuje diastolická dysfunkce. Diastolická dysfunkce může začít již v časném stadiu onemocnění (zejména z hlediska poměru E/e´ ) a postupně se s progresí onemocnění zhoršuje.
Specifičtější je skvrnitý vzor (myokardu), který se objevuje v důsledku rozdílné echogenity mezi amyloidními depozity a myokardem.
Kromě toho je senzitivním a specifickým nálezem pro srdeční amyloidózu specifický obraz globálního longitudiálního strainu (GLS). GLS se obvykle snižuje dříve než LVEF, což vede k disociaci GLS-LVEF. V důsledku toho lze vypočítat poměr LVEF:GLS a použít jej k odlišení srdeční amyloidózy od jiných patologií s podobným vzhledem.
Obraz GLS typicky bez postižení apikálních segmentů.
Video 6 Amyloidóza srdce, projekce PLAX - Pacient s potvrzenou AL amyloidózou s typickými echokardiografickými známkami amyloidové infiltrace myokardu. Na videu níže jsou vidět hypertrofická boční stěna a interventrikulární septum s charakteristickým zrnitým nebo skvrnitým vzhledem myokardu a poruchou hybnosti bazálních segmentů LK.

Obrázek 14 Zrnitý vzhled myokardu IVS sekundárně v důsledku ukládání amyloidu, projekce PLAX. Příčinou je hyperechogenita amyloidových depozit ve srovnání s okolním myokardem.

Obrázek 15 Planární průměry levé komory, PLAX projekce - všimněte si koncentrické hypertrofie levé komory, která není při EDD 44 mm dilatovaná, ale má hypertrofické septum (13 mm) a laterální stěnu (12 mm). Patrný je také skvrnitý vzhled myokardu.

Video 7 AL amyloidóza, apikální čtyřdutinová projekce - zrnitý myokard, ztluštělé stěny LK a snížená pohyblivost bazálních segmentů.

Video 8 Další pacient s potvrzenou AL amyloidózou, PLAX projekce - koncentrická hypertrofie LK se zachovanou ejekční frakcí a bez zjevné regionální poruchy hybnosti.

Video 9 TTR amyloidóza, A4C projekce - pokročilá forma amyloidózy s granulovaným jiskřením myokardu, LK má koncentrickou hypertrofii s průměrem IVS 14 mm. Všimněte si také hypokinezy bazálních segmentů (šetřící apikální segmenty).

Obrázek 16 PW Dopplerovské měření mitrálního průtoku u pacienta s amyloidózou - všimněte si restriktivního tvaru signálu mitrálního přítoku s dominantní vlnou E a poměrem E/A 4,17 ukazujícím na těžkou diastolickou dysfunkci (stupeň III-IV) způsobenou infiltrací myokardu amyloidem.

Obrázek 17 Stupeň diastolické dysfunkce na základě signálu mitrálního přítoku

Obrázek 18 Septální (levá strana) a laterální (pravá strana) maximální časná diastolická rychlost mitrálního prstence (e′) - všimněte si snížených rychlostí vln s', e' a a', které jsou nižší než 5 cm/s. Poměr E/e' 28,9 významně poukazuje na zvýšené plnicí tlaky s odpovídající diastolickou dysfunkcí.

Obrázek 19 Systolická exkurze roviny trikuspidálního prstence (TAPSE) měřená v režimu M, AL amyloidóza, projekce A4C - všimněte si snížené systolické exkurze na 14 cm, která je rovněž známkou zhoršeného pohybu bazálních segmentů sekundárně v důsledku amyloidózy.

Obrázek 20 Měření globálního longitudiálního strainu (GLS) u pacienta s amyloidózou - zobrazen typický obraz strainu pro amyloidózu s apikální úsporou, nejlépe patrný na bulls-eye diagramu. Snížená podélná kontrakce v bazálních segmentech - GLS 7 %.

Obrázek 21 Měření globálního longitudiálního strainu (GLS), AL amyloidóza - typicky bez postižení apikálních segmentů, GLS -11 %.

Magnetická rezonance srdce (CMR)
CMR může být vysoce vypovídající o srdeční amyloidóze, nelze ji však použít ke stanovení konečné diagnózy.
Měla by být použita v případě klinického podezření, že příčinou zvýšené tloušťky stěny by mohl být infiltrativní proces, hypertrofická kardiomyopatie, konstriktivní perikarditida nebo myokarditida.
Kromě toho CMR nedokáže rozlišit různé typy amyloidu a je třeba použít jiné diagnostické metody (viz níže).
Mezi nálezy CMR svědčící pro srdeční amyloidózu patří zesílení biventrikulárního a síňového septa a normální velikost komorové dutiny.
LGE obvykle odhalí difuzní nebo skvrnité subendokardiální zesílení, které často zahrnuje síně, a také zvýšení extracelulárního objemu při T1 vážení.
Diagnostická kritéria ESC jsou shrnuta níže (Obrázek 22).

Garcia-Pavia P, Rapezzi C, Adler Y, et al. Diagnosis and treatment of cardiac amyloidosis: a position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2021 Apr 21;42(16):1554-1568. doi: 10.1093/eurheartj/ehab072. PMID: 33825853; PMCID: PMC8060056.
Laboratorní testování
Rutinní laboratorní vyšetření mohou odhalit postižení různých orgánů, například abnormální jaterní testy - postižení jater nebo abnormální ledvinové testy - postižení ledvin.
Natriuretické peptidy (BNP, NT-proBNP) nebo srdeční troponiny jsou zvýšené při postižení srdce.
K diagnostice AL amyloidózy je třeba stanovit přítomnost lehkých řetězců.
Mezi testy, které se doporučuje provést, patří: koncentrace volných lehkých řetězců v séru, imunofixační elektroforéza séra a moči (IFE) a analýza poměru volných lehkých řetězců kappa/lamda v séru.
Před provedením nukleárních zobrazovacích metod pro potvrzení diagnózy ATTR by měla být vyloučena AL amyloidóza.
Nukleární zobrazovací metody
Nukleární zobrazování hraje klíčovou roli při potvrzení ATTR amyloidózy. K posouzení vychytávání technecia v srdci se používá scintigrafie s kostním tracerem (PYP, DPD nebo HMDP, především v závislosti na dostupnosti). Pozitivní vyšetření je definováno jako vychytávání 2. nebo 3. stupně nebo poměr H/CL > 1,5. Pokud je nukleární zobrazovací test dostupný, odpadá nutnost provedení srdeční biopsie a v současné době se jedná o preferovanou metodu vzhledem k nižšímu riziku pro pacienta.
Endomyokardiální biopsie
Endomyokardiální biopsie (EMB) byla standardní metodou pro potvrzení diagnózy srdečního amyloidu. S rozvojem neinvazivního testování se však její role snížila. Lze ji zvážit u pacientů s neprůkaznými výsledky předchozích vyšetření nebo v případě pochybností o diagnóze srdeční amyloidózy. Ve standardních případech se lze EMB vyhnout.
Obrázek 23 Diagnostika amyloidózy

AL označuje lehký řetězec imunoglobulinu; ATTRv - srdeční varianta transtyretinové amyloidózy; ATTRwt - transtyretinová amyloidóza divokého typu; CMR - magnetická rezonance srdce; H/CL - poměr srdce/kontralaterální hrudník; HCM - hypertrofická kardiomyopatie a IFE - imunofixační elektroforéza.
Kittleson MM, Maurer MS, Ambardekar AV, et al. American Heart Association Heart Failure and Transplantation Committee of the Council on Clinical Cardiology. Cardiac Amyloidosis: Evolving Diagnosis and Management: A Scientific Statement From the American Heart Association. Circulation. 2020 Jul 7;142(1):e7-e22. doi: 10.1161/CIR.0000000000000792. Epub 2020 Jun 1. Erratum in: Circulation. 2021 Jul 6;144(1):e11. PMID: 32476490.
Terapie
Existují dvě možné oblasti terapie srdeční amyloidózy. První je zvládání srdečního selhání a druhou je léčba samotné amyloidózy, pokud je to možné.
Léčba srdečního selhání
K léčbě srdečního selhání vyvolaného srdeční amyloidózou lze použít standardní farmakologickou léčbu srdečního selhání. Pacienti však nemusí tolerovat hypotenzi, která je důsledkem užívání inhibitorů angiotenzin konvertujícího enzymu, blokátorů angiotenzinových receptorů, inhibitorů neprilyzinu a angiotenzinových receptorů, beta-blokátorů a antagonistů mineralokortikoidních receptorů. Obvykle se předepisují kličková diuretika.
Antiarytmická léčba
V současné době chybí údaje týkající se antiarytmické léčby u pacientů se srdeční amyloidózou. U těchto pacientů je několik odlišných rysů. Pokud je na základě zobrazovacích metod podezření na dysfunkci síní, mohou pacienti profitovat z antikoagulační léčby, a to i v případě nepřítomnosti fibrilace/flutteru síní. Problematickou oblastí je používání implantabilních kardioverterů-defibrilátorů (ICD), protože pacienti nemusí profitovat z jejich implantace. Důvodem je skutečnost, že častou příčinou srdeční zástavy u těchto pacientů je nedefibrilovatelný rytmus. Použití ICD by mělo být zváženo u pacientů s dokumentovanou komorovou arytmií. Neexistují však žádné definitivní informace, které by podpořily jednoznačné doporučení.
Transplantace srdce
Transplantace srdce představuje možnou terapeutickou cestu, její použití však má řadu omezení. To proto, že amyloidóza je často multiorgánové onemocnění a amyloidogenní protein má také zdroj, který je vždy mimo srdce. Je třeba provádět pečlivý výběr pacientů. U AL amyloidózy je třeba transplantaci srdce kombinovat s léčbou základního onemocnění, která zahrnuje chemoterapii. U amyloidózy ATTRm se zdroj nachází v játrech, a proto je jedinou schůdnou možností kombinovaná transplantace srdce a jater. U amyloidózy ATTRwt není transplantace srdce obvykle indikována, protože obvykle postihuje starší pacienty, kteří pro ni nesplňují věková kritéria.
Specifická terapie AL amyloidózy
Léčbu AL amyloidózy provádí hematolog. Existují dvě hlavní terapeutické možnosti: chemoterapie a/nebo autologní transplantace kmenových buněk.
Specifická léčba ATTR amyloidózy
Kromě výše zmíněné transplantace jater nebo kombinované transplantace srdce a jater pro léčbu dědičné ATTR se objevily nové možnosti léčby ATTRwt. Tafamidis je vhodný pro pacienty s ATTR kardiomyopatií se srdečním selháním klasifikovaným podle New York Heart Association jako třída I až III.
Tafamidis působí jako stabilizátor transtyretinu a snižuje tvorbu amyloidu. Tafamidis snižuje úmrtnost a hospitalizace související s kardiovaskulárními chorobami, zlepšuje kvalitu života a snižuje pokles funkční kapacity. Pro použití u pacientů s neuropatií vyvolanou amyloidózou schválila FDA další léky.
Sarkoidóza
Sarkoidóza je zánětlivé granulomatózní onemocnění, které může postihnout jakýkoli orgán.
Až u čtvrtiny pacientů se systémovou sarkoidózou se může objevit známky postižení srdce.
Zánětlivý proces vede k jizvení, které nejčastěji postihuje interventrikulární septum, zadní část levé komory, pravou komoru a přední část levé komory.
Mezi klinické projevy srdeční sarkoidózy patří AV blokády, síňové arytmie, komorové arytmie a srdeční selhání.
Echokardiografické nálezy - ztenčení bazální stěny IVS nebo volné stěny LK, aneuryzmata stěny, poruchy pohybu stěny a diastolická dysfunkce jsou typickými projevy srdeční sarkoidózy.
MR srdce - LGE typicky přítomen ve střední stěně a/nebo epikardu, vynechávající subendokard (bazální část srdce, zejména septum a laterální stěnu)
F18 FDG-PET - je užitečné pro detekci a odpověď na léčbu.
Definitivní diagnóza vyžaduje patologické potvrzení nekaseifikujícího granulomu endomyokardiální biopsií, ačkoli senzitivita je nízká.
Imunosuprese kortikosteroidy zůstává standardní léčbou akutní zánětlivé fáze.
Video 10 Sarkoidóza srdce s aneuryzmatem bazální části inferoseptální stěny, modifikovaná A4C projekce - všimněte si výrazné hypokinezy inferoseptální stěny a bazálních částí laterální stěny. LK není dilatovaná s odhadovanou EF 50 %.

Obrázek 24 Sarkoidóza, průměr inferoseptálního aneuryzmatu - 28 x 14 mm.

Video 11 Sarkoidóza srdce s aneuryzmatem bazální části inferoseptální stěny, projekce PSAX

Video 12 Sarkoidóza srdce s aneuryzmatem bazální části inferoseptální stěny, projekce A4C - všimněte si hypokinetického pohybu bazálních částí.

Obrázek 25 Hodnocení globálního longitudinálního strainu u sarkoidózy - GLS snížena na -14,5 %, výrazná hypokineze bazálních částí inferoseptální stěny (aneuryzma).

Video 13 Srdeční sarkoidóza, projekce A4C - středně dilatovaná LK s LVEF 45-50 % a aneuryzmatem bazální ⅓ interventrikulárního septa. Postižené části jsou akinetické či dyskinetické.

Video 14 Srdeční sarkoidóza, projekce PLAX - aneuryzma interventrikulárního septa.

Hemochromatóza
Srdeční hemochromatóza neboli primární kardiomyopatie z přetížení železem je důležitou a potenciálně preventabilní příčinou srdečního selhání.
Syndromy přetížení železem mohou být dědičné nebo získané.
Zpočátku je charakterizována diastolickou dysfunkcí nebo arytmiemi - k ukládání železa může docházet v celém převodním systému srdce, zejména v atrioventrikulárním uzlu (úplná atrioventrikulární blokáda může vyžadovat implantaci trvalého kardiostimulátoru).
Paroxysmální fibrilace síní je nejčastější arytmií pozorovanou u pacientů se srdeční hemochromatózou. Prevalence komorových arytmií se zvyšuje s dilatací levé komory a nízkou LVEF.
V pozdějších stadiích může onemocnění přejít v dilatační kardiomyopatii.
Terapie stavů přetížení železem je důležitá pro prevenci nebo zvrácení srdeční dysfunkce. Odstranění přebytečného železa z tkání u těchto pacientů minimalizuje tvorbu volných radikálů, což snižuje orgánové poškození.
Terapie k odstranění nadbytečných zásob železa zahrnuje terapeutickou flebotomii a látky chelatující železo.
Při léčbě srdeční hemochromatózy jsou důležité také dietní opatření.
Městnavé srdeční selhání by mělo být léčeno standardní medikamentózní terapií pro srdečního selhání.
Video 15 Hereditární hemochromatóza způsobující HFrEF, PLAX projekce - hemochromatóza způsobující difuzní hypokinézu, hrot a dolní stěna jsou téměř akinetické, biplanární EF 16 %. LS je těžce dilatovaná (LAVi 75,4 cm3/m2).

Video 16 Dědičná hemochromatóza způsobující HFrEF, PSAX projekce

Video 17 Hereditární hemochromatóza způsobující HFrEF, projekce A3C - difuzní hypokineze až akineze, EF 16 %.

Video 18 Hereditární hemochromatóza způsobující HFrEF po léčbě (2 letý follow up), pohled PLAX - normalizace velikosti a funkce LK (EF 55-60 %), bez významných regionálních poruch pohybu stěn.

Video 19 Dědičná hemochromatóza způsobující HFrEF po léčbě (2 letý follow up), pohled A4C - normalizace velikosti a funkce LK (EF 55-60 %), žádné významné regionální abnormality pohybu stěn.

Zdroje
- Zipes, Peter Libby, Robert O. Bonow, Eugene Braunwald. Braunwald's Heart Disease : a Textbook of Cardiovascular Medicine. Philadelphia, PA :Elsevier/Saunders, 2015
- Georgios Papingiotis; Lamprini Basmpana, Dimitrios Farmakis, Cardiac amyloidosis: epidemiology, diagnosis and therapy, e-Journal of Cardiology Practice, Vol. 19, N° 19 - 21 Apr 2021, available from: https://www.escardio.org/Journals/E-Journal-of-Cardiology-Practice/Volume-19/cardiac-amyloidosis-epidemiology-diagnosis-and-therapy
- Kittleson MM, Maurer MS, Ambardekar AV, Bullock-Palmer RP, Chang PP, Eisen HJ, Nair AP, Nativi-Nicolau J, Ruberg FL; American Heart Association Heart Failure and Transplantation Committee of the Council on Clinical Cardiology. Cardiac Amyloidosis: Evolving Diagnosis and Management: A Scientific Statement From the American Heart Association. Circulation. 2020 Jul 7;142(1):e7-e22. doi: 10.1161/CIR.0000000000000792. Epub 2020 Jun 1. Erratum in: Circulation. 2021 Jul 6;144(1):e11. PMID: 32476490.
- https://www.wikidoc.org/index.php/Cardiac_amyloidosis_echocardiography
- Agha AM, Parwani P, Guha A, Durand JB, Iliescu CA, Hassan S, Palaskas NL, Gladish G, Kim PY, Lopez-Mattei J. Role of cardiovascular imaging for the diagnosis and prognosis of cardiac amyloidosis. Open Heart. 2018 Sep 26;5(2):e000881. doi: 10.1136/openhrt-2018-000881. Erratum in: Open Heart. 2018 Nov 21;5(2):e000881corr1. PMID: 30305910; PMCID: PMC6173267.
- Garcia-Pavia P, Rapezzi C, Adler Y, Arad M, Basso C, Brucato A, Burazor I, Caforio ALP, Damy T, Eriksson U, Fontana M, Gillmore JD, Gonzalez-Lopez E, Grogan M, Heymans S, Imazio M, Kindermann I, Kristen AV, Maurer MS, Merlini G, Pantazis A, Pankuweit S, Rigopoulos AG, Linhart A. Diagnosis and treatment of cardiac amyloidosis: a position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2021 Apr 21;42(16):1554-1568. doi: 10.1093/eurheartj/ehab072. PMID: 33825853; PMCID: PMC8060056.
- Adler Y, Charron P, Imazio M, et al.; ESC Scientific Document Group. 2015 ESC Guidelines for the diagnosis and management of pericardial diseases: The Task Force for the Diagnosis and Management of Pericardial Diseases of the European Society of Cardiology (ESC)Endorsed by: The European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2015 Nov 7;36(42):2921-2964.
.jpg)


